|
Основы термодинамики.
Макроскопические тела обладают внутренней эенергией, которя равна сумме кинетических энергий беспорядочного движения и потенциальных энергий взаимодействия друг с другом всех молекул тела. Внутренняя энергия является однозначной функцией термодинамических параметров: температуры и объема.В случае идеального одноатомного газа внутрення энергия зависит только от температуры: 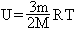 . .В случае многоатомного газа в данной формуле вместо числа 3 будет число 2n+1, где n - число атомов в молекуле газа. Согласно первому закону термодинамики изменение внутренней энергии системы при переходе из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданного системе: dU=A+Q. Работа, совершаемая над системой, в термодинамике равна A=-p.dV, где p - давления, а dV - изменение объема. Сама система при этом совершает работу A`=-A. При нагревании и охлаждении количество теплоты равно Q=cm.dT, где c - удельная теплоемкость, а dT - изменение температуры. Кроме того теплота поглощается при парообразовании и плавлении и выделяется при конденсации и кристализации. Работа и количество теплоты - характеристики процессов, при которых происходит изменение внутренней энергии системы.
При изохорном процессе (V=const) работа равна нулю и dU=Q.
При изотермическом процессе (T=const) внутренняя энергия идеального газа не меняется и Q=A`.
При изобарном процессе (p=const) передаваемая системе теплота идет на изменение внутренней энергии системы и совершение работы: Q=dU+A`.
При адиабатном процессе (в теплоизолированной системе) Q=0, dU=A.
При обмене теплотой в теплоизолированной системе без совершения работы выполняется уравнение теплового балланса: Q1+Q2+Q3+...Qn=0, где Q - количества теплоты полученные или отданные телами системы. Процесссы, протекающие в природе с макроскопическими телами, необратимы. Типичные необратимые процессы таковы: теплота самопризвольно переходит от горячего тела к холодному, но не наоборот; механическая энергия самопроизвольно переходит во внутреннюю.
Путем обобщения опытных фактов, касающихся необратимости процессов, был сформулирован второй закон термодинамики. Из законов термодинамики вытекает, что тепловые двигатели могут совершать работу только в процессе передачи теплоты от нагреватлея к холодильнику. Максимально возможное значение коэффициента полезного действия теплового двигателя равно: 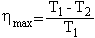 ,где T1 - температура нагревателя, T2 - температура холодильника. ,где T1 - температура нагревателя, T2 - температура холодильника.
Повышение КПД тепловых двигателей, приближение его к максимально возможному - важнейшая техническая задача.

С вопросам и предложениями обращаться на marklv25@mail.ru
| 
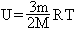 .
.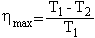 ,
,