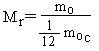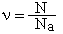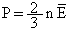|
Основы молекулярно-кинетической теории.
Согласно основным положениям МКТ все тела состоят из молекул (или атомов); между молеклами на малых расстояниях (меньших размеров молекул) действуют силы отталкивания, а на больших - силы притяжения; молекулы участвуют в хаотичном тепловом движении.  Массы молекул малы, а число их в макроскопических телах огромно. Поэтому вместо абсолютных значений масс молекул и их количества вещества в макроскопических телах используют относительные величины. Относительной молекулярной (или атомной) массой называют отношение массы молекулы (или атома) к 1/12 массы атома углерода. 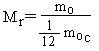 Количество вещества выражается в молях. Моль- количество вещества, содержащее столько же молекул, сколько содержиться атомов в 0,012 кг углерода.
Число молекул в моле вещества называют постоянной Авогадро: NA=6.1023 моль-1.
Количество вещества равно отношению числа молекул N в теле к постоянной Авогадро. 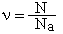 Молярной массой называют массу вещества, взятого в количестве одного моля. M = moNA В газах расстояние между молекулами во много раз больше размеров последних. В жидкостях и твердых телах молекул (или атомы) находятся непосредственно друг возле друга. В твердых телах атомы (или молекулы) расположены в строгом порядке и совершают колебания около неизменных положений равновесия. В жидкостях молекулы расположены неупорядоченно и время от времени совершают перескоки из одного положения равновесия в другое. В МКТ идеальным газом называют газ, состоящий из молекул, взамимодействием которых можно пренебречь.
Согласно основному уравнению МКТ давление газа пропорционально произведению концентрации молекул на среднюю кинетическую энергию поступательного движения молекулы. 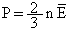

  
С вопросам и предложениями обращаться на marklv25@mail.ru
|